2021年12月m6A RNA甲基化研究领域的10分以上文章有14篇,现精选部分研究的主要结果供大家阅读欣赏。

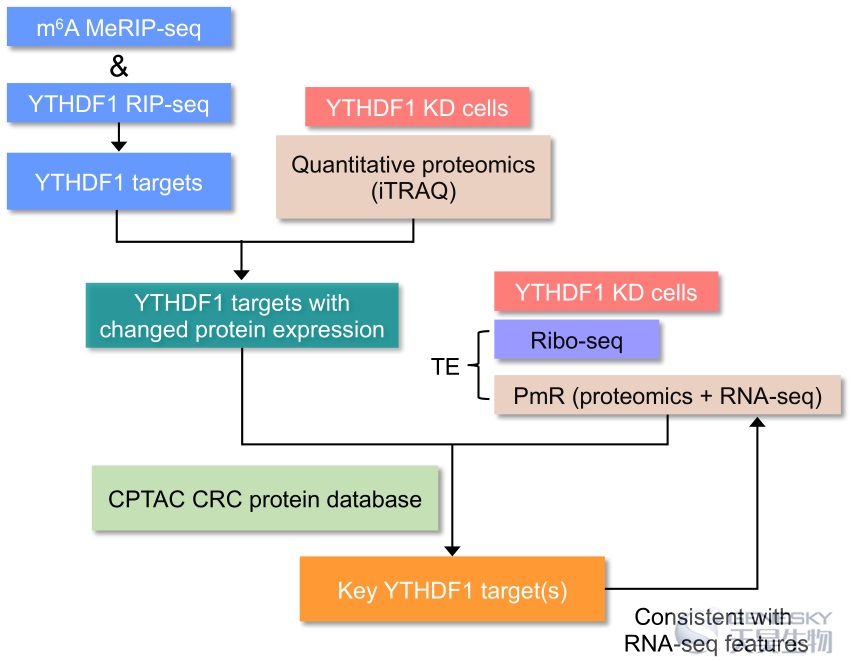
m6A通过m6A识别蛋白控制RNA的命运。结直肠癌(CRC)表现出异常的m6A修饰和m6A调控因子的表达。然而,m6A识别蛋白如何解释致癌m6A甲基组促进恶性转化仍有待阐明。结果发现YTHDF1的DNA拷贝数增加是CRC的常见事件,与其过表达有关。YTHDF1高表达与患者肿瘤中的转移性基因特征显著相关。在小鼠中敲除Ythdf1可以抑制炎症性CRC模型中的肿瘤生长。YTHDF1在体内促进CRC细胞系和原代类器官的细胞生长及肺、肝转移。综合多组学分析发现RhoA激活剂ARHGEF2是YTHDF1的关键下游靶点。YTHDF1结合到ARHGEF2 mRNA的m6A位点,导致ARHGEF2翻译增强。ARHGEF2的异常表达在体外体内恢复了YTHDF1缺失引起的RhoA信号通路受损、细胞生长和转移能力,证实了ARHGEF2是YTHDF1的关键靶点。最后,脂质纳米粒子(LNP)递送的ARHGEF2 siRNA在体内显著抑制肿瘤生长和转移。因此,本研究发现了YTHDF1-m6A-ARHGEF2的一个新的致癌表观转录组轴调控CRC的肿瘤发生和转移。转运siRNA的LNP药物证实了靶向这一轴在结直肠癌中的治疗潜力。

近年来的研究发现,m6A水平在几种癌症类型的外周血中存在显著的异常调节,并具有诊断价值。然而,基于m6A修饰的角度,还没有建立一个用于准确筛查多种癌症类型的生物标志物。本研究的目标是开发一种基于m6A靶miRNAs的血清诊断特征,用于肿瘤的大规模检测。共纳入14965份血清样本,包括12种癌症类型。基于训练集(n=7299),作者使用支持向量机算法开发了用于癌症检测的m6A-miRNAs特征。m6A-miRNAs特征具有较高的准确性,其在训练集、内部验证集和外部验证集中的曲线下面积(AUC)分别达到0.979、0.976和0.936。在区分癌症类型方面,m6A-miRNAs特征在每一种癌症类型中都表现出了优越的灵敏度,在识别肺癌、胃癌和肝细胞癌时具有令人满意的AUC。此外,m6A-miRNAs的诊断性能不受性别、年龄和良性疾病的干扰。总之,本研究揭示了血清循环m6A miRNAs在癌症检测中的价值,并为RNA修饰等新型精准、低成本、低侵袭性的肿瘤大规模筛查生物标志物的开发提供了新的方向和策略。

YTHDC1作为核m6A 识别蛋白在调节RNA代谢中具有独特的功能。这项研究发现YTHDC1在急性髓系白血病(AML)中过表达,并且它是人类AML细胞增殖和生存所必需的。Ythdc1基因的缺失显著阻碍小鼠体内AML的发生和维持以及白血病干细胞(LSCs)的自我更新。另外发现Ythdc1也是体内正常造血和造血干细胞和祖细胞(HSPC)维持所必需的。值得注意的是,Ythdc1单倍剂量不足在体内降低LSCs的自我更新,但不会降低HSPCs的自我更新。敲低YTHDC1对原代AML细胞增殖有较强的抑制作用。在机制上,YTHDC1通过MCM4调控白血病的发生,MCM4是DNA复制的关键调控因子。这项研究提供了令人信服的证据,表明YTHDC1在AML中具有致癌作用和独特的机制。

环状RNA (circRNA)被报道涉及多种疾病,然而,其在过敏性皮炎(AD)或银屑病中的作用尚不清楚。这项研究试图确定健康对照组和AD患者外周血单个核细胞(PBMCs)中circRNAs的差异表达谱,并探讨circRNAs在AD发病中的潜在作用机制。结果从88750个circRNAs中鉴定出一个功能未知的circRNA hsa_circ_0004287,该circRNA在AD和银屑病患者的PBMCs中均上调,且在炎症条件下主要由巨噬细胞表达。hsa_circ_0004287在体外抑制M1巨噬细胞的活化,巨噬细胞特异性过表达hsa_circ_0004287可减轻AD和银屑病样小鼠的皮肤炎症。机制上,hsa_circ_0004287通过m6A依赖的方式竞争性结合IGF2BP3和MALAT1,降低了其宿主基因MALAT1的稳定性。MALAT1水平的降低促进了S100A8/S100A9的泛素化降解,从而阻碍了p38/MAPK的磷酸化和巨噬细胞介导的炎症反应。因此hsa_circ_0004287在AD和银屑病中以m6A依赖的方式抑制M1巨噬细胞激活,可作为AD和银屑病的通用治疗候选药物。

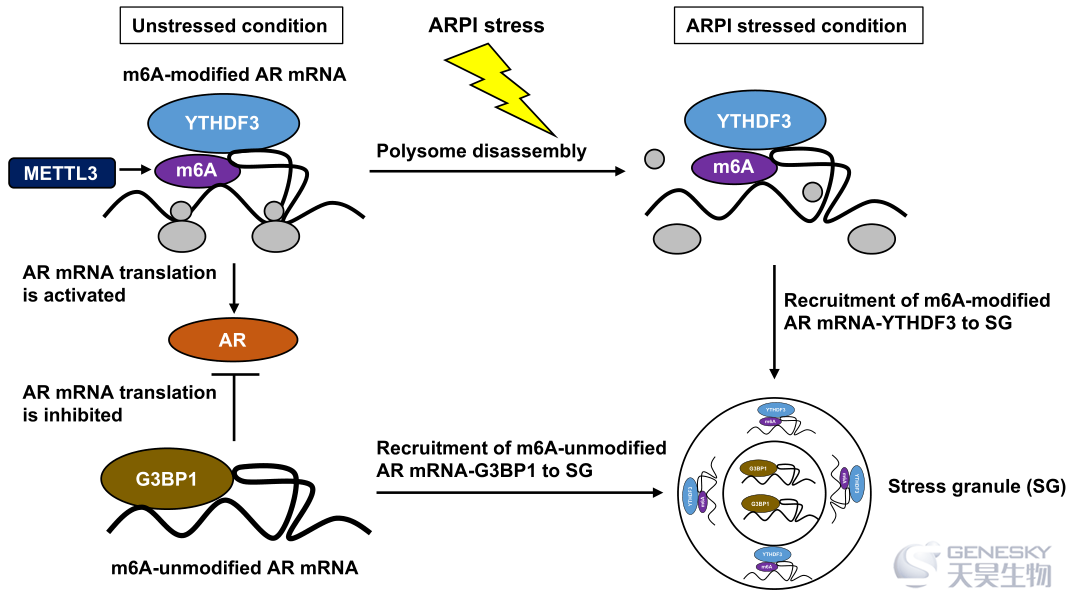
这项研究报道了前列腺癌(PCA)中雄激素受体(AR) mRNA调控和细胞保护的新机制,以应对AR通路抑制(ARPI)应激。AR mRNA的翻译受RNA结合蛋白YTHDF3和G3BP1的调控。在环境条件下,m6A修饰的AR mRNA被YTHDF3结合并受到翻译刺激,而m6A未修饰的AR mRNA被G3BP1结合并受到翻译抑制。当AR调控的PCA细胞株受到ARPI应激时,m6A修饰的AR mRNA从积极翻译的多聚体(PSs)被募集到RNA-蛋白应激颗粒(SGs),导致AR mRNA翻译减少。ARPI应激后,m6A修饰的AR mRNA与YTHDF3液相分离,而m6A未修饰的AR mRNA与G3BP1相分离。因此,这些AR mRNA信息在SGs中形成了两个不同的YTHDF3富集或G3BP1富集的簇。ARPI诱导的SG形成具有细胞保护作用,当YTHDF3或G3BP1沉默阻止时,会增加PCA细胞的死亡,以应对ARPI应激。有趣的是,AR mRNA的沉默也延迟了ARPI应激诱导的SG的形成,突出了其在触发这种应激反应中的支持作用。这一研究结果为ARPI应激后的应激适应细胞生存定义了一种新的机制,包括SG调控的AR mRNA的翻译,由m6A RNA修饰及其各自的调节蛋白所介导。

RNA分子经历了大量的化学转录后修饰(PTMs),可以影响其结构和相互作用的性质。近年来,越来越多的PTMs通过依赖高通量测序的实验方法成功地比对到转录组上。牛津纳米孔直接RNA测序已被证明对RNA修饰敏感。这一研究开发并验证了Nanocompore,这是一个强大的分析框架,可以识别这些数据的修饰。其策略是将感兴趣的RNA样本与未修饰的对照样本进行比较,不需要训练集,并允许重复使用。结果发现Nanocompore可以在体外检测到不同的RNA修饰,并具有位置准确性,将其应用于酵母和人类RNA以及靶向非编码RNA的体内m6A谱。作者用正交方法证实了研究结果,并为单个RNA分子上的多个修饰残基共现提供了新的见解。

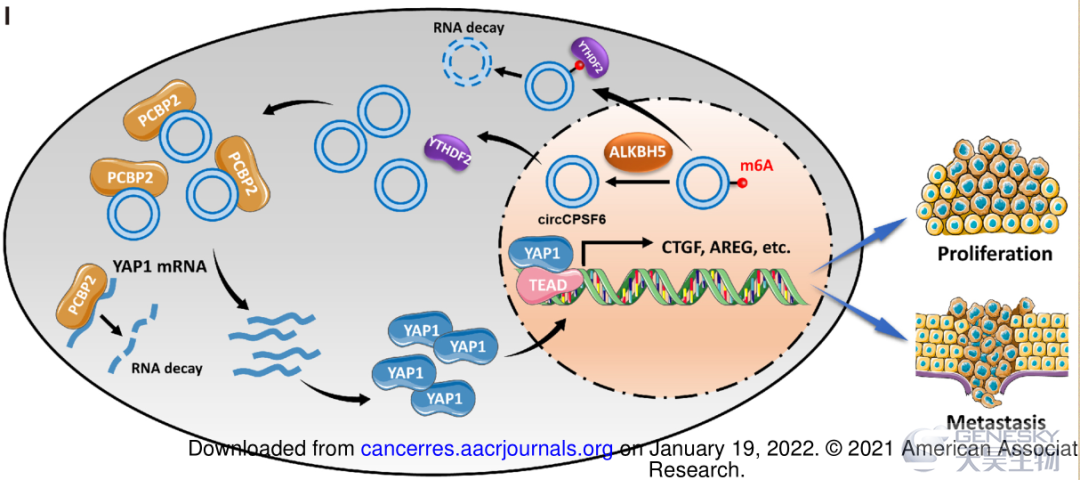
circRNA和m6A修饰广泛参与多种肿瘤的进展,包括肝细胞癌(HCC)。然而,circRNA和m6A之间的联系在HCC的发病机制中仍不明确。作者研究了HCC中m6A介导的circRNA调控。通过整合两项已发表的研究的信息,鉴定了m6A相关的circRNA,发现环状切割和聚腺苷酸化特异性因子6(circCPSF6)是一种新的m6A修饰的circRNA。CircCPSF6主要受ALKBH5介导的去甲基化影响,其次为YTHDF2的识别和失稳作用。同时,在HCC标本中circCPSF6表达上调,而circCPSF6表达升高可作为肝癌患者生存恶化的独立预后因子。功能缺失检测表明,circCPSF6维持了细胞增殖和致瘤性,并增强了细胞运动性和肿瘤的转移。CircCPSF6触发YAP1的表达,进一步激活其下游的级联。在机制上,circCPSF6竞争性地结合PCBP2,减弱其与YAP1 mRNA的结合,从而维持YAP1的稳定性。在体外和体内,去除YAP1在功能上逆转了circCPSF6的作用。circCPSF6-YAP1轴的异常激活促进了肝癌的恶性。这些发现为研究m6A修饰对circRNA的调控以及这种表观遗传重编程在HCC中的作用提供了新的视角。

天昊生物具有多年基因组、转录组和表观组等多组学检测与分析的经验,m6A RNA甲基化作为表观领域的一大热点,天昊生物自主设计了m6A调控因子(writers/erasers/readers)差异表达分析检测panel,还可以提供m6A修饰整体水平定量检测,并结合MeRIP-seq和RNA-seq挖掘受m6A调控因子影响的下游靶点,同时可对相关的靶点进行MeRIP-qPCR验证。生信团队亦可提供个性化的m6A数据库挖掘与生信分析内容。
咨询沟通请联系
18964693703(微信同号)

创新基因科技,成就科学梦想

 咨询热线:400-065-6886
咨询热线:400-065-6886

 咨询热线:400-065-6886
咨询热线:400-065-6886












