
 咨询热线:400-065-6886
咨询热线:400-065-6886

 咨询热线:400-065-6886
咨询热线:400-065-6886
砷不仅是一种有毒金属,也是一种环境应激源,广泛存在于地下水、大气和土壤中。流行病学研究表明,母体砷暴露增加了成年后代患2型糖尿病的风险。然而,早期生命的砷暴露导致成人代谢性疾病的潜在机制仍不清楚。
表观遗传重编程是早期生命暴露于不利环境压力源与晚年健康结局之间关联的一种潜在机制。5-甲基胞嘧啶(5mC)是DNA甲基化的一种形式,通过10-11易位(TET)双加氧酶家族被氧化为5-羟甲基胞嘧啶(5hmC),5hmC参与DNA去甲基化过程。研究发现5hmC在肝脏中富集。然而到目前为止,尚无关于环境胁迫下代谢疾病特异性基因5hmC修饰的研究报道。
因此,为了研究生命早期暴露于砷对成年期葡萄糖和脂质代谢的影响,安徽医科大学卫生毒理学系徐德祥团队从DNA羟甲基化重编程角度揭示了β-氧化相关基因羟甲基化修饰介导了成年小鼠早期砷诱发的肝脏脂质积累。相关研究成果于2022年2月18日发表在Journal of Hazardous Materials杂志上(IF:10.588)。

天昊生物为本研究中的表观遗传研究提供了特色的多重目的区域甲基化和和羟甲基化测序技术服务,下边让我们看看文章的主要结果吧!
作者首先研究了早期砷暴露对于小鼠成年期代谢的影响。结果发现砷暴露小鼠在出生时体重低于对照,出生后三周内体重追赶上对照组(如下图A, C);暴露组小鼠运动降低(图B, D),而换气比值增加;并且也分别比较了暴露组和对照组雄性和雌性后代不同部位白色脂肪组织的重量差异。
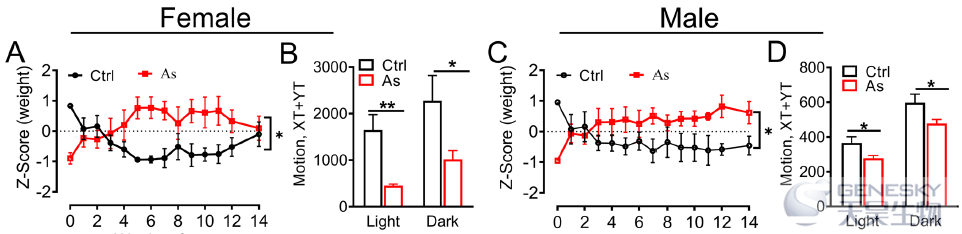
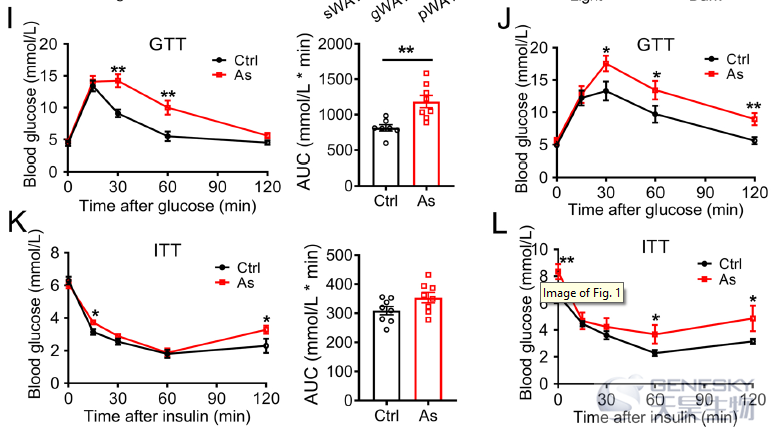
糖耐量实验显示砷暴露的成年后代曲线下面积(AUCs)显著增加(如下图I, J)。胰岛素耐量实验显示对成年雌性后代的胰岛素耐受性没有影响,而砷暴露的成年雄性后代曲线下面积显著增加(图K, L)。同时,砷暴露的成年后代血清胰岛素升高。这些结果说明早期砷暴露会导致成年后的葡萄糖和胰岛素耐受性。
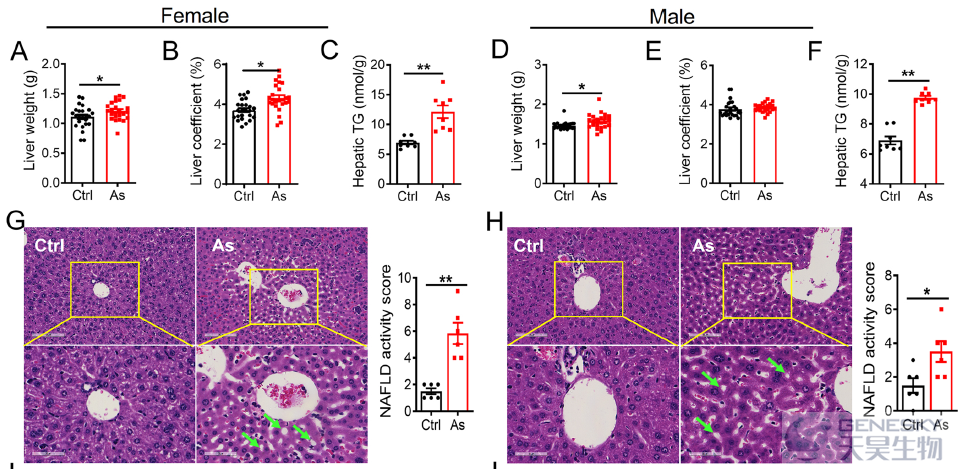
作者进一步分析发现在早期暴露后,成年后代的肝损伤。暴露组绝对的肝重量更高,尽管相对的肝脏重量/体重仅在雌性暴露组增加。另外,暴露组肝脏甘油三酯(TG)含量增加(如下图A-F)。HE染色显示暴露组的非酒精性脂肪性肝病(NAFLD)活性评分高于对照组(图G, H)。
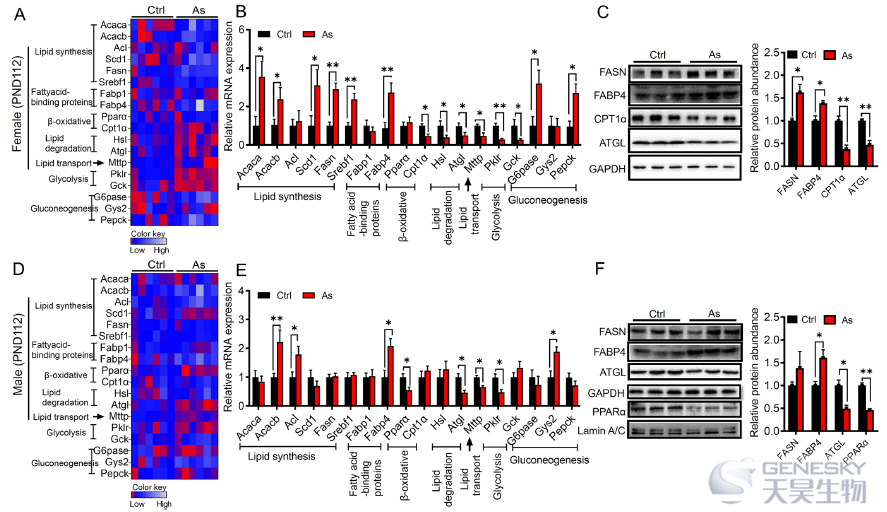
然后,作者利用RT-qPCR技术分别分析了雌性成年后代和雄性后代在早期砷暴露后肝脂质和糖代谢相关基因的表达差异,并且利用免疫印迹对一些基因的蛋白水平进行分析,发现了部分基因在RNA和蛋白水平上的变化趋势一致,包括FASN、FABP4、CPT1α、ATGL、PPARα(如下图)。
为了探讨早期砷暴露是否对成年小鼠肝脏脂代谢相关基因表观遗传重编程产生影响,作者利用LC-MS/MS发现暴露组5mC和5hmC在基因组水平上并没有显著改变。利用天昊生物多重目的区域甲基化测序技术MethylTarget®对肝脏脂代谢相关基因Fasn, Srebf1, Cpt1α, Pparα, Atgl和Mttp的5mC修饰水平进行分析,发现部分基因的CpG片段甲基化水平发生改变(如下图A-D)。同时,利用天昊生物基于ACE-seq自主设计的多重目的区域羟甲基化测序技术分析了这些基因的5hmC水平,部分片段的羟甲基化水平也发生了显著变化(如下图E-H)。

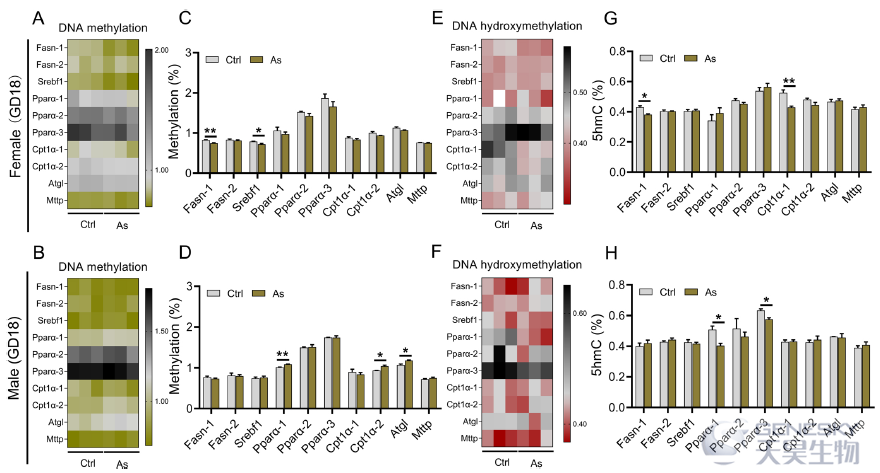
接下来,作者也分析了胎儿期肝脏脂代谢相关基因的DNA甲基化和羟甲基化水平变化。砷暴露雄性小鼠肝脏中基因组水平5mC降低,雌性和雄性小鼠基因组水平5hmC水平均降低。对特定基因的分析也发现β-氧化相关基因5mC和5hmC水平发生改变(如下图)。
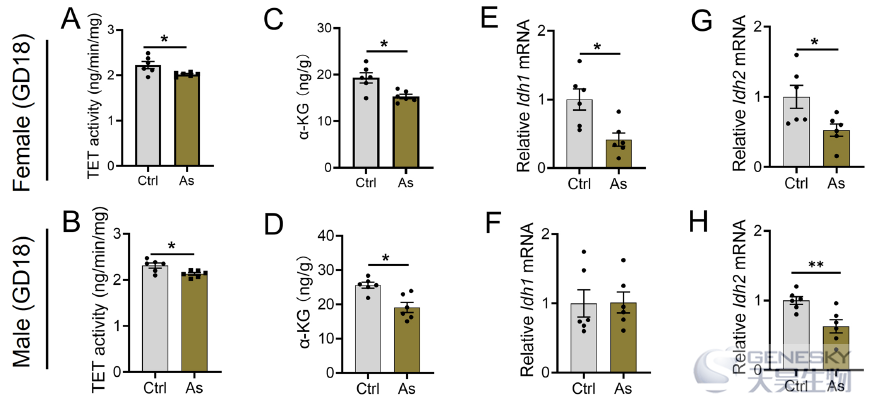
TET家族包括TET1、TET2和TET3,是α-酮戊二酸(α-KG)依赖的双加氧酶,其作用是催化DNA羟甲基化。对胎儿肝脏中TET活性进行检测,发现暴露组中TET活性降低(如下图A, B),α-酮戊二酸水平相应降低(图C, D)。异柠檬酸脱氢酶1 (Idh1)和2 (Idh2)是线粒体α-KG合成的两个关键基因。RT-PCR检测发现砷暴露的雌性胎儿肝脏中Idh1和Idh2 mRNA表达下调(图E-H)。
利用ChIP-qPCR分析TET1和肝脏Cpt1α和Pparα启动子CpG富集区域的结合能力(如下图I, L)。发现Cpt1α和Pparα的CpG区直接结合到TET1(图J, M)。TET1与肝脏Cpt1α启动子的第一个CpG片段结合,在砷暴露的雌性胎儿中减少。相应地,砷暴露的雌性胎儿肝脏Cpt1α mRNA减少;而砷暴露的雄性胎儿肝脏Pparα mRNA减少(图K, N)。

总结来看,本研究探讨了早期环境应激源砷暴露对成年后代肝脏脂质代谢的影响。发现早期砷暴露导致成年期肝脏脂质积累,部分是因为胎儿肝脏中β-氧化相关基因的DNA羟甲基化重编程改变。在机制上,生命早期暴露于砷抑制β-氧化相关基因的5hmC修饰部分是通过抑制TET与CpG片段的结合以及降低发育的肝脏中α-KG依赖的TET活性。这项研究表明早期生命的环境压力通过改变胎儿发育中的DNA羟甲基化重编程导致后期代谢紊乱。

创新基因科技,成就科学梦想